Bis zu zehn Prozent aller Menschen in Deutschland leiden an einer chronischen Nierenerkrankung. Da die Niere eine zentrale Rolle in der Körperhomöostase spielt, haben Betroffene ein deutlich erhöhtes Risiko für eine Vielzahl von Erkrankungen, inklusive für Herz-Kreislauf-Erkrankungen wie Herzinfarkt und Schlaganfall.
Die IgA-Nephropathie, die häufigste entzündliche Nierenerkrankung, schreitet trotz optimierter Standardtherapie bei bis zu einem Drittel der Patient:innen bis zum vollständigen Verlust der Nierenfunktion fort. Neue, in der Pathophysiologie der Erkrankung spezifisch eingreifende Medikamente, zeigen ein heterogenes Ansprechen, was darauf hindeutet, dass es verschiedene Unterformen („Endotypen“) der Erkrankung gibt, die bislang nicht ausreichend verstanden sind.
Eine wesentliche Hürde war bisher die technische Limitierung herkömmlicher Mikroskopieverfahren, mit denen nur wenige molekulare Proteinmarker gleichzeitig untersucht werden konnten. Um diese Einschränkung zu überwinden, haben wir an unserem Standort mehrere neuartige molekulare Mikroskopiemethoden entwickelt und etabliert.
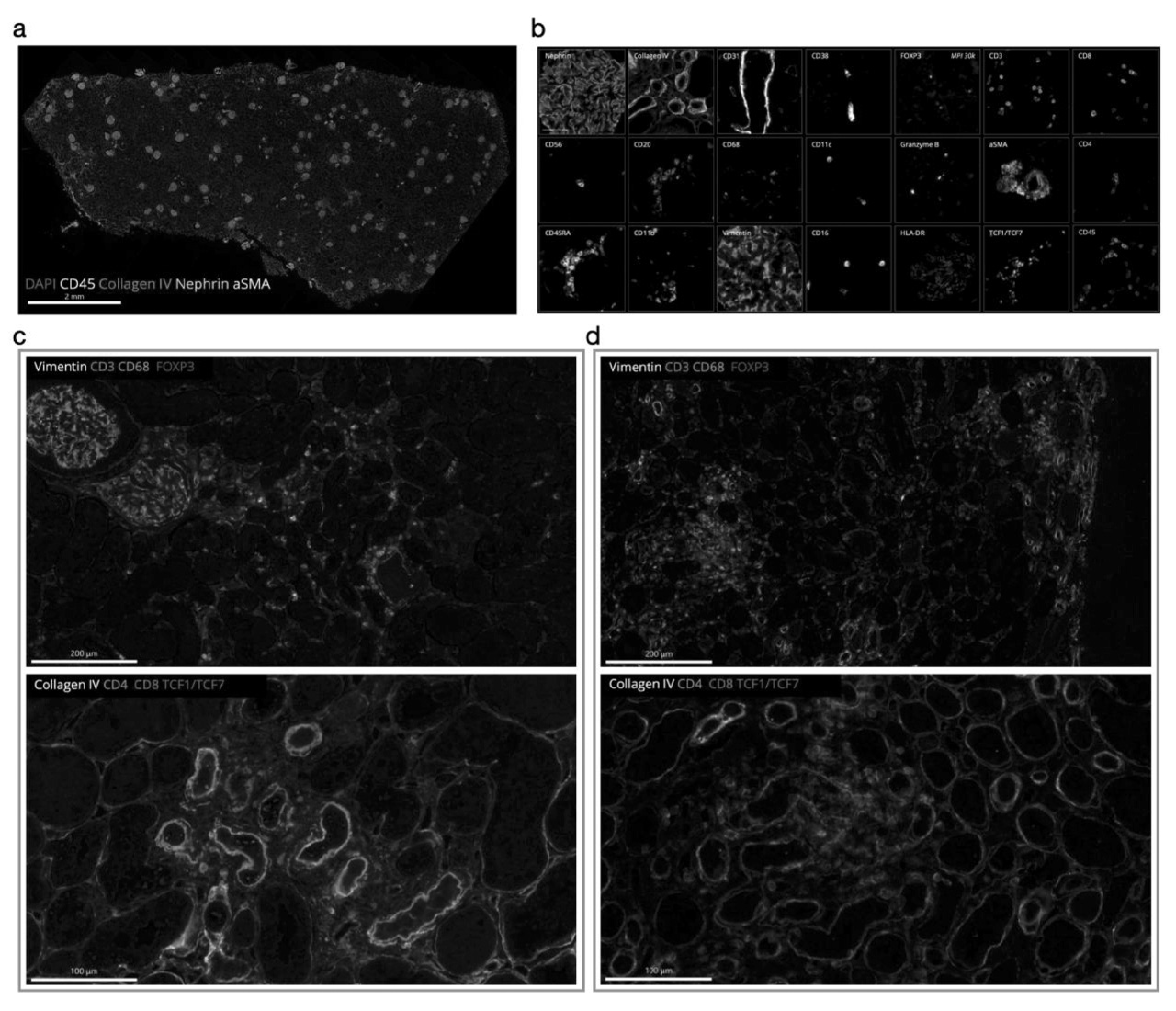
Diese Technologien (insbesondere „Spatial Proteomics“, Abbildung 1) erlauben es, >100 Proteine gleichzeitig im Gewebe zu analysieren und dabei Zelltypen, Signalwege und Gewebearchitektur zu visualisieren. Dadurch können unterschiedliche molekulare Krankheitsformen, etwa entzündlich vs. narbig-fibrotisch, erstmals gewebebasiert identifiziert werden. Das Ziel ist, künftig gezielt jene Therapie auszuwählen, die für die individuelle Patientin oder den individuellen Patienten den größten Nutzen bietet und gleichzeitig unnötige Kosten und Nebenwirkungen zu vermeiden.
Am Universitätsklinikum Hamburg-Eppendorf bestehen dafür ideale Voraussetzungen: Mit der HERO-Biobank und dem Hamburger GN-Register stehen international einzigartige klinische Kohorten und Biomaterialien zur Verfügung. Das Projekt hilft somit, die führende Rolle des UKE in der nephrologischen Präzisionsmediz zu stärken und den Weg zu einer individuelleren, wirksameren Behandlung dieser weltweit relevanten Erkrankung zu ebnen.