Projektförderung durch die Treuhandstiftung, Huckfeldt-Weber Kinderstiftung.
Der Begriff „Neuronale Ceroid-Lipofuszinosen“ (NCL) fast eine Gruppe von fatalen Speichererkrankungen zusammen, die vornehmlich im Kindesalter auftreten und umgangssprachlich auch als Kinderdemenz bezeichnet werden.
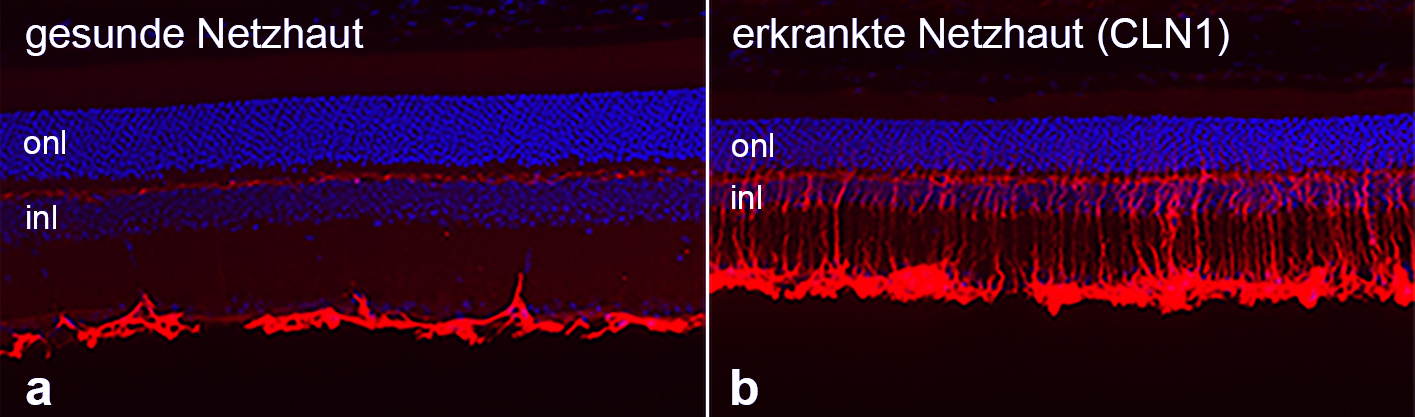
Es ist die häufigste erblich bedingte neurodegenerative Erkrankung bei Kindern und Jugendlichen. Ursache dieser Erkrankungen sind Fehlfunktionen bestimmter Zellorganellen, der Lysosomen, die für den Abbau von zellfremdem und zelleigenem Material verantwortlich sind. Als Folge dieser Fehlfunktion sammelt sich schädlicher „Müll“ in den Zellen an, und es kommt zu einem rasch fortschreitenden Verlust von Nervenzellen im Gehirn und in der Netzhaut. Als Folge hiervon verlieren die betroffenen Kinder die Fähigkeit zu gehen, zu denken und zu sprechen sowie ihre Sehkraft bis hin zur Erblindung.
Für eine bestimmte NCL Erkrankung gibt es bereits eine Möglichkeit, die Neurodegeneration im Gehirn zu behandeln. Behandlungsmöglichkeiten für den fortschreitenden Verlust von Nervenzellen in der Netzhaut und der daraus resultierenden Erblindung existieren gegenwärtig jedoch noch nicht.
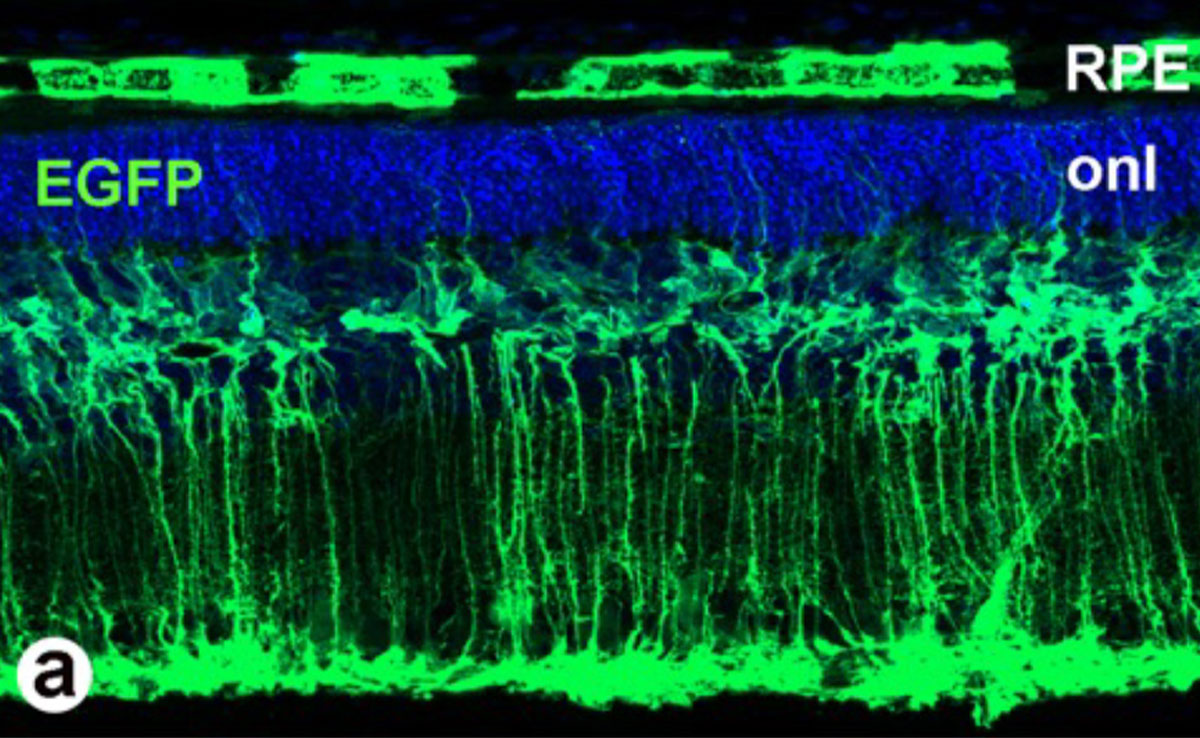
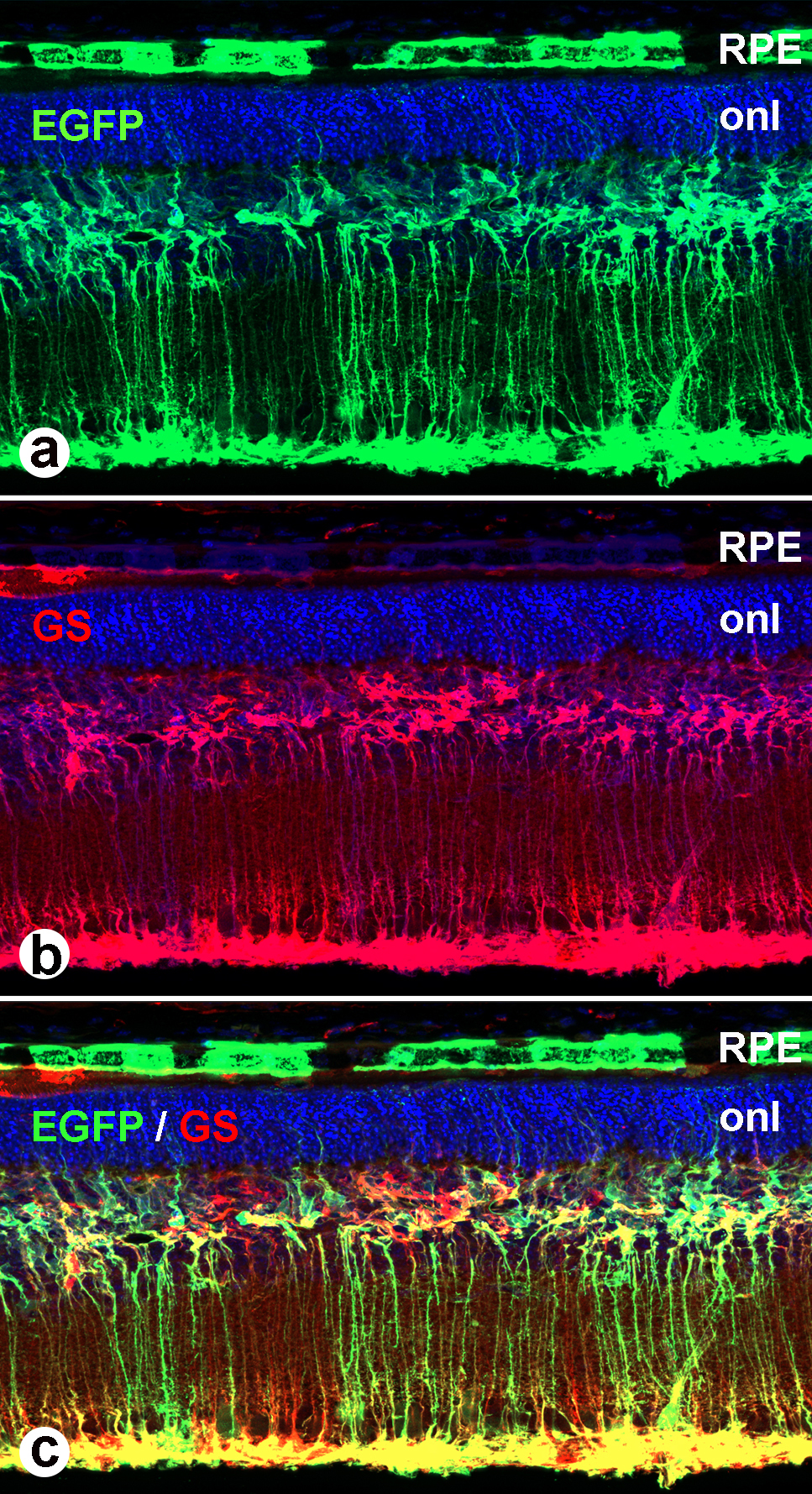
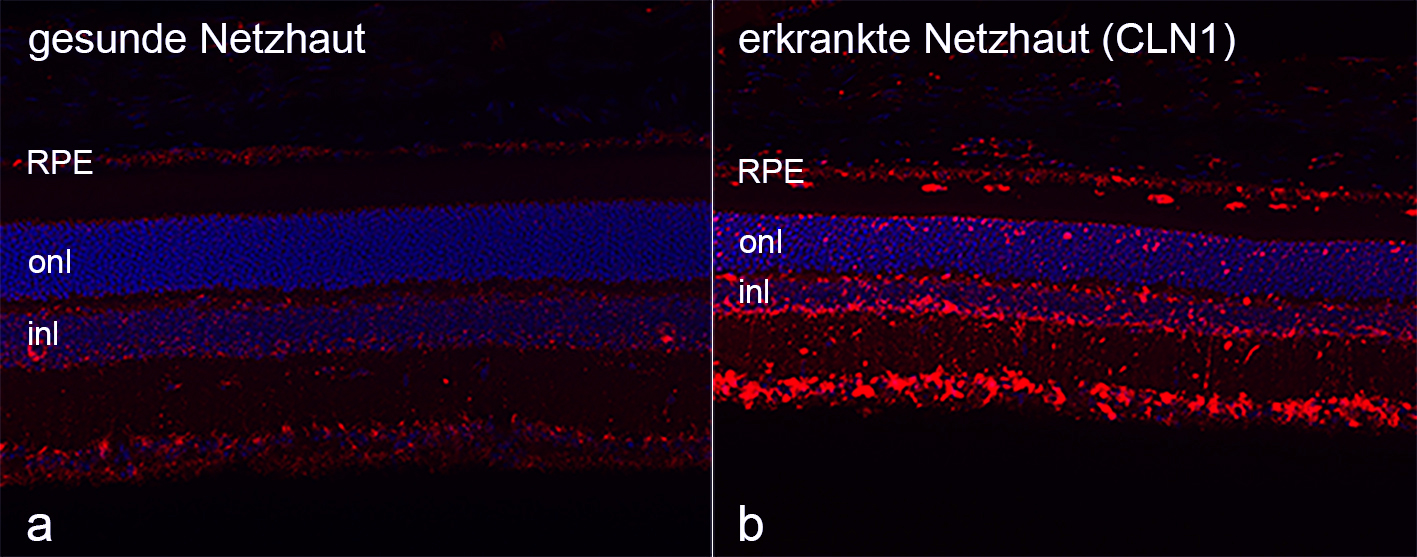
Ziel des Projektes ist es, die Degeneration der Netzhaut und den Verlust der Sehkraft durch eine Enzymersatzstrategie zu verlangsamen oder eventuell sogar aufzuhalten. Dieses wird in dieser Arbeit in einem Mausmodell für eine bestimmte NCL-Form, der CLN1 Erkrankung versucht. Über einen Vektorvermittelten Gentransfer soll in der Netzhaut dieses Tiermodells eine funktionale Variante eines bei dieser Erkrankung nicht funktionsfähigen Enzyms produziert werden. Dieses Enzym kann dann von den umliegenden Nervenzellen aufgenommen und zu den Lysosomen transportiert werden. Im Idealfall könnte so die Fehlfunktion der Lysosomen korrigiert und damit die Ursache der Erkrankung behoben werden.
Erster Zwischenbericht
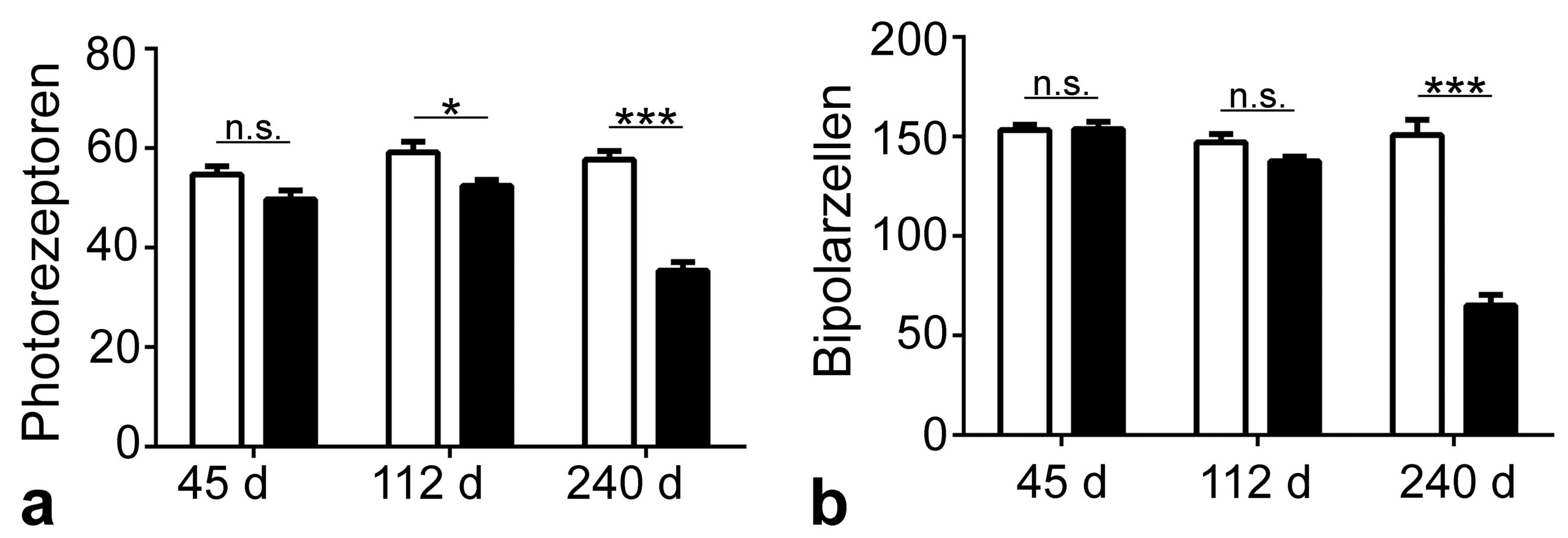
In den letzten 12 Monaten konnten wir dank der Förderung durch die Huckfeldt-Weber Kinderstiftung die Erforschung einer Gentherapie für die Behandlung von NCL – bekannt als „Kinderdemenz“ – anstoßen. Diese Erkrankung führt zum bisher unheilbaren Erblinden dieser Kinder. Ziel der Forschungsarbeit ist es, dieses Erblinden zu verzögern oder gar zu verhindern. Als wichtigstes Ergebnis der bisher durchgeführten Arbeiten konnte ein deutlich verlangsamter Funktionsverlust der Netzhaut im Tierexperiment nachgewiesen werden. Der geförderte Gentherapieansatz stellt nach den bisherigen Ergebnissen eine vielversprechende Behandlungsstrategie dar, die Struktur und Funktion der Netzhaut der betroffenen Patient:innen zu erhalten.